Terug naar het richtlijnenoverzicht
Deze richtlijn is gebaseerd op de “KHA-CARI Guideline recommendations for renal biopsy (Nephrology 201916)” uit Australië en Nieuw-Zeeland, de “CIRSE Standards of Practice on Peri-operative Anticoagulation Management During Interventional Radiology Procedures 2021 (Cardiovascular and interventional radiology6)” uit Europa, de “Update on the Native Kidney Biopsy: Core Curriculum 2019 (Am J Kidney Dis 201915)” en “The Native Kidney Biopsy: Update and Evidence for Best Practice (Clin J Am Soc Nephrol. 20168)” beide uit de Verenigde Staten. Tot op heden was er vanuit de Nederlandse Federatie Nefrologie geen richtlijn voor het verrichten van een natieve nierbiopsie en hanteert ieder ziekenhuis zijn eigen protocol. In de KHA-CARI Guideline wordt gebruik gemaakt van de GRADE systematiek die zo veel mogelijk overgenomen is. Echter, het aantal adviezen dat berust op goede kwaliteit onderzoek is beperkt waardoor er slechts een zeer beperkt aantal evidence based adviezen gegeven kunnen worden. Derhalve zijn deze adviezen aangevuld met practice points op basis van expert-opinion uit de geraadpleegde literatuur waarbij alleen artikelen van na 2010 zijn gebruikt (figuur 1).
De vetgedrukte adviezen zijn in aangepaste vorm afgeleid van de adviezen uit de 4 onderliggende Engelstalige richtlijnen waarbij de adviezen met GRADE classificatie alleen afkomstig zijn uit de KHA-CARI guideline. Waar nodig hebben wij in cursief gedrukte tekst toelichting gegeven op basis van deze richtlijnen. Normaal gedrukt commentaar is gebaseerd op expert opinion uit Nederland.
Figuur 1 Toepassing van practice points (uit: KDIGO)

Lijst van afkortingen
|
ADP-remmer |
Adenosinedifosfaat remmer |
|
aPTT |
Geactiveerde Partiele Tromboplastine Tijd |
|
BMI |
Body Mass Index |
|
BMS |
Bare metal stent |
|
CT-A |
CT Angiografie |
|
CVA |
Cerebro Vasculair Accident |
|
DAPT |
Duale antiplaatjestherapie |
|
DES |
Drug eluting stent |
|
DOAC |
Directe Orale Anticoagulantia |
|
eGFR |
Estimated glomerular filtration rate |
|
Hb |
Hemoglobine |
|
INR |
International Normalized Ratio |
|
LMWH |
Laagmoleculairgewicht heparine |
|
LTA |
Landelijke Transmurale Afspraak |
|
NSAID |
Non-Steroidal Anti-Inflammatory Drugs |
|
PFA |
Platelet Function Analyzer |
|
PTT |
Protrombinetijd |
|
RLC |
Richtlijncommissie |
|
TAR |
Trombocytenaggregatie remmer |
|
VKA |
Vitamine K antagonisten |
Deze leidraad bevat aanbevelingen van algemene aard voor de nefrologische voorbereiding en nabewaking bij een natief nierbiopt. Verder bevat de leidraad adviezen voor de technische uitvoering van het nierbiopt voor nefrologen die zelf de nierbiopsie uitvoeren. Voor technische uitvoering door radiologen wordt verwezen naar de richtlijnen van de Nederlandse Vereniging voor Radiologie, die niet betrokken is geweest bij de inhoud van deze richtlijn en deze richtlijn ook niet geautoriseerd heeft. Het is mogelijk dat in een individueel geval deze aanbevelingen niet van toepassing zijn. Het is de verantwoordelijkheid van de behandelend arts te beoordelen of de leidraad in de praktijk toepasbaar is. Er kunnen zich feiten of omstandigheden voordoen waardoor, in het belang van een goede zorg voor de patiënt, van deze adviezen moet worden afgeweken.
1.1 Verstrek patiënten en hun naasten informatie over de procedure van de nierbiopsie inclusief de reden van de biopsie, de te verwachten gevolgen, mogelijke risico’s en praktische informatie waar de patiënt op de dag van en periode na de biopsie rekening mee moet houden. Hierbij moet aandacht worden geschonken aan eventuele angst voor de biopsie (1C).
Onderbouwing:
Zie bijlage 1 met voorbeeld voor standaardtekst voor patiënteninformatie. Deze tekst dient te worden aangepast aan de lokale situatie. Zie bijlage 2 met de checklist voor hulpverleners (uit: KNMG; informed consent) waaraan moet worden voldaan voor volledige informatie voorziening aan de patiënt.
1.2 Overweeg om een nierbiopsie te verrichten bij patiënten met nierinsufficiëntie, proteïnurie en/of hematurie. Een nierbiopsie wordt alleen uitgevoerd indien nu of in de toekomst het beleid hierdoor wordt bepaald (practice point).
Tabel 1: Indicaties voor nierbiopsie (uit: Update on the Native Kidney Biopsy, Luciano 201915)
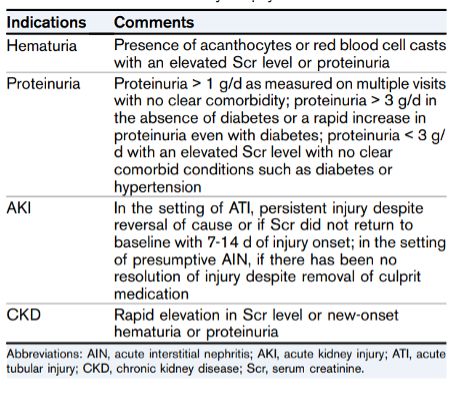
Onderbouwing:
In tabel 1 wordt een overzicht van mogelijke indicaties voor nierbiopsie weergeven. Er is geen GRADE classificatie aangehouden gezien voor iedere indicatie een wisselende mate van bewijs is te vinden. Verder is de timing van het biopsie afhankelijk van de context en beloop van een casus.
1.3 Evalueer patiënten voor potentiële contra-indicaties die het risico op een bloeding verhogen na de nierbiopsie (practice point).
Onderbouwing:
In tabel 2 wordt een overzicht van contra-indicaties voor nierbiopsie weergeven. Er is geen GRADE classificatie aangehouden aangezien voor iedere contra-indicatie een wisselende mate van bewijs is te vinden. Indien de patiënt voldoet aan één of meerdere contra-indicaties moet worden overwogen of indicatie zwaarder weegt dan de contra-indicatie(s).
Tabel 2: Mogelijke contra-indicaties voor nierbiopsie (uit: The Native Kidney Biopsy: Update and Evidence for Best Practice, Hogan 20168) .

1.4 Meet de bloeddruk voorafgaand aan de nierbiopsie waarbij in een electieve setting een bloeddruk < 140/90 mmHg moet worden nagestreefd voorafgaand aan én de eerste 24 uur na de de nierbiopsie om het risico op een bloeding te minimaliseren. Indien dit niet wordt bereikt, moet, afhankelijk van de urgentie van de stellen diagnose en daarmee samenhangende behandelconsequenties, worden overwogen de biopsie uit te stellen (practice point).
Commentaar:
Momenteel is er geen consensus in de literatuur omtrent de streef bloeddruk voorafgaand aan een nierbiopsie. De meta-analyse van Corapi et al.3 toonde een verhoogd bloedingsrisico na nierbiopsie bij een systole > 130 mmHg (1.4% versus 0.1%) wat niet significant was maar wel klinisch relevant. Kriegshauser et al.12 beschreef in een retrospectieve studie dat bij een systole > 140 mmHg de kans op bloedingscomplicaties (transfusie of interventie) 10x groter was in vergelijking met een systole < 140 mmHg. Een diastole > 90 mmHg was ook geassocieerd met meer complicaties. Feldman et al.4 beschreef in een retrospectieve studie dat het risico op hematoomvorming significant toenam bij een systole > 155 mmHg. Echter, in deze studie zijn ook biopten uit transplantaatnieren meegenomen in de analyse.
In de Amerikaanse update van Hogan et al. 8 uit 2016 wordt aangegeven dat een verhoogd risico op een bloeding vooral bepaald wordt door voorgeschiedenis met hypertensie. Desondanks wordt op basis van de literatuur door Hogan et al8 geadviseerd om een streef bloeddruk te hanteren van < 140/90 mmHg en in ieder geval niet te biopteren bij bloeddruk > 160/100 mmHg. Om kans op bloeding na de nierbiopsie te verminderen dient de eerste 24 uur na de nierbiopsie ook een bloeddruk < 140/90 nagestreefd te worden.
Tevens dient er aandacht te worden besteed aan eventuele angst voor de biopsie wat met oxazepam 10mg zo nodig kan worden behandeld.
1.5 Verricht de volgende bepalingen met daarbij de aanbevolen streefwaarden: Hb (> 5.0 mmol/l), trombocyten (> 50 × 109/l), normale PTT en aPTT en bij gebruik van VKA de INR (< 1.5) (practice point).
Onderbouwing:
Bij een trombocytopenie kan een biopsie alleen veilig plaatsvinden als het trombocyten aantal is gecorrigeerd tot > 50 × 109/l en eventuele anemie bij voorkeur gecorrigeerd tot Hb > 5.0 mmol/l. Verder is een uitgangswaarde voor het Hb belangrijk om bij follow-up van het Hb adequaat te kunnen handelen. De RLC acht het niet noodzakelijk om bij iedere patiënt een kruisproef en bloedgroep te bepalen voorafgaand aan de biopsie. Indien er verdenking is op een bloeding kan dit alsnog worden gedaan bij afname van de follow-up Hb waarde.
In de CIRSE richtlijn6 wordt geadviseerd om de PTT te verrichten in plaats van de INR omdat de INR is ontwikkeld voor patiënten die VKA gebruiken. De PTT kan ook verlengd zijn bij andere condities (bv. leverlijden, stollingsziekte, medicatie etc.)
1.6 Verricht niet standaard bij alle patiënten een PFA test voorafgaande aan een nierbiopsie (practice point)
Onderbouwing:
De RLC acht het op basis van onderstaande literatuurgegevens NIET noodzakelijk om bij alle patiënten voorafgaande aan een nierbiopsie een PFA test te verrichten. In geen van de onderliggende guidelines/updates wordt de PFA gebruikt als screening voor stolling. Van den Hoogen et al.9 heeft aangetoond dat een verlengde PFA een betere voorspeller was voor bloedingen dan de bloedingstijd. Echter, het corrigeren hiervan leidde niet tot minder bloedingen en er waren ook bloedingen gerapporteerd bij patiënten met een normale PFA. Daarbij komt dat er meer macroscopische hematurie werd gezien zonder ernstige complicaties. Islam et al. rapporteerde geen associatie tussen een verlengde PFA en het optreden van een bloeding. Derhalve adviseren wij om niet routinematig de PFA-test toe te passen.
Echter, bij patiënten met preterminale nierinsufficiëntie, dialysepatiënten en patiënten met erfelijke vormen van trombopathie kan een PFA test wel worden overwogen. Bij verlengde PFA kan er gekozen worden om af te zien van nierbiopsie of te kiezen voor transjugulaire benadering, echter met dit laatste is maar bij een zeer beperkt aantal centra expertise.
Indien bij een verlengde PFA toch wordt besloten een biopsie te verrichten kan een eenmalige desmopressine dosering volstaan zonder dat de PFA opnieuw hoeft te worden gecontroleerd. Het advies is om desmopressine 1 uur voor de biopsie te geven. De dosering voor desmopressine is 0.3 ug/kg en leidt meestal niet tot een klinisch relevante hyponatriëmie als patiënten het advies van vochtbeperking (1.5L per dag) gedurende de dag van de biopsie volgen.
Mekawy et al.17 toonden aan dat hemodialyse leidt tot een gedeeltelijke correctie van een verlengde PFA. Bij dialyse patiënten kan dit effect dus worden toegepast in plaats van of als aanvulling op desmopressine.
1.7 De RLC verwijst voor adviezen met betrekking tot continueren/staken van antistolling naar de website van de LTA (https://lta-antistollingszorg.nl/) en onderstaande aanvullende adviezen van de RLC over continueren of staken van acetylsalicylzuur afhankelijk van risico op cardiovasculaire events (practice point).
Onderbouwing:
Aangezien het beleid rondom antistolling met enige regelmaat wijzigt heeft de RLC besloten om in dit protocol grotendeels de landelijke LTA adviezen te volgen. Een nierbiopsie valt onder de overige chirurgie en behoort tot een hoog-risico ingreep.
Ten tijde van publicatie van deze richtlijn is de meest opvallende wijziging in het antistollingsbeleid van de LTA dat van de antiplaatjes middelen alleen de acetylsalicylzuur / carbasalaatcalcium gecontinueerd kan worden. Tot op heden werd geadviseerd alle vormen van antiplaatjes therapie zo veel mogelijk te staken voor nierbiopsie. De RLC is van mening dat er op basis van de LTA en de beperkte beschikbare literatuur van niet gerandomiseerde en retrospectieve onderzoeken (Kumar. 2018, Fontana 2023) en de CARI richtlijn (MacGinley. 2019) geen overtuigende aanwijzingen zijn dat het risico op grote bloedingen verhoogd is bij continueren van acetylsalicylzuur. Derhalve lijken de voordelen van continueren van ascal voor een nierbiopsie bij patiënten met een hoog risico op cardiovasculaire events op te wegen tegen het mogelijke risico op bloedingen. Bij patiënten met een laag risico op cardiovasculair event adviseert de RLC de acetylsalicylzuur minimaal 5 dagen voor de biopsie te staken indien de indicatie voor de nierbiopsie uitstel toelaat om zodoende risico op bloeding te minimaliseren, met name bij patiënten met verhoogd risico op bloedingen waaronder patiënten met fors gestoorde nierfunctie, hemodialyse, suboptimale bloeddruk en verlaagd aantal bloedplaatjes. De risico’s van continueren van acetylsalicylzuur (kans op bloeding) en tijdelijk onderbreken daarvan (kans op ischemisch event) dienen met de patiënt te worden besproken.
Dit hoofdstuk is alleen van toepassing voor nefrologen die zelf de nierbiopsie uitvoeren. De Nederlandse Vereniging voor Radiologie is niet betrokken geweest bij de inhoud van deze richtlijn en heeft deze richtlijn ook niet geautoriseerd.
2.1 Gebruik een veergedreven, automatische biopteur voor nierbiopsie aangezien deze zijn geassocieerd met minder complicaties en betere biopten (1B).
Onderbouwing:
De keuze welke nier gebiopteerd moet worden is afhankelijk van de kliniek. Veelal is er sprake van twee echografisch normaal uitziende nieren waardoor er op nefrologisch gebied geen voorkeur is en zal de nefroloog samen met de patiënt besluiten welke zijde de voorkeur heeft. In geval van een schrompelnier zal er uiteraard in de andere nier gebiopteerd moeten worden.
2.2 Overweeg een 16G naald voor de nierbiopsie te gebruiken aangezien deze naald de beste keuze lijkt in de balans tussen een goed beoordeelbare biopsie en het risico op bloedingen (2C).
Onderbouwing:
Meestal volstaat het om 2 biopten af te nemen waarbij de nefroloog kan besluiten om een extra biopsie te nemen indien getwijfeld wordt aan de kwaliteit van de eerdere biopten.
2.3 Overweeg bij patiënten met leverfalen / levercirrose of bij patiënten met een harde indicatie voor continueren van antistolling een transjugulair biopsie te verrichten indien dat mogelijk is in het centrum (of te verwijzen naar een centrum met dergelijke mogelijkheden). Het alternatief is om een percutaan biopsie te verrichten waarbij slechts 1 biopt wordt afgenomen (practice point).
Onderbouwing:
Een patiënt met leverfalen heeft een verhoogd risico op een bloeding vanwege een trombocytopenie, trombocytopathie en/of verlengde PTT. Patiënten met levercirrose hebben bovendien een verhoogd risico op bloedingen na de biopsie ondanks optimalisatie van de risico factoren.
2.4 Verricht een percutaan nierbiopsie altijd onder geleide van beeldvorming met de voorkeur voor echografische geleiding (1B).
2.5 Biopteer de patiënt (indien mogelijk) bij voorkeur in buikligging met een zandzak onder de buik en bij voorkeur in de onderpool van de nier (practice point).
Onderbouwing:
Bij voorkeur wordt er een biopsie verricht in de onderpool van de nier aangezien de kans op het raken van de grote arteriën dan het kleinste is.
2.6 Overweeg om een patiënt met milde respiratoire insufficiëntie of morbide obesitas (BMI > 30 kg/m2) in zijligging te biopteren (2B).
2.7 Overweeg om bij uitzonderlijke situaties (geïntubeerde patiënten, zwangerschap, trauma etc) de positie te kiezen die zo optimaal mogelijk is om te biopteren waarbij rekening wordt gehouden met het comfort van de patiënt (practice point).
3.1.1 Beoordeel de conditie van de patiënt en mogelijke contra-indicaties op de dag van de biopsie (practice point).
Onderbouwing:
Er dient voornamelijk te worden gecontroleerd of de patiënt fit genoeg is voor een nierbiopsie en of de patiënt voldoet aan de veiligheidscriteria voor de biopsie (stolling en bloeddruk).
3.1.2 Probeer om voorafgaand aan een electieve nierbiopsie een stabiele bloeddruk van < 140/90 mmHg te bereiken. Indien dit na enkele medicamenteuze pogingen niet wordt bereikt, overweeg dan om de biopsie uit te stellen als er geen sprake is van een spoedindicatie (practice point).
Onderbouwing:
Zie toelichting bij hoofdstuk 1.1.4
3.1.3 Verricht bij opname een controle van het Hb (streef > 5 mmol/l) indien de meest recente waarde > 2 weken geleden bepaald is of indien de patiënt in de tussenliggende periode ziek is geweest. Een bloedtransfusie dient te worden overwogen bij een Hb < 5 mmol/l met nadien controle van de opbrengst (practice point).
Onderbouwing:
Een Hb controle voorafgaand aan de biopsie dient laagdrempelig overwogen te worden. Bij een Hb controle na een gecompliceerde biopsie kan dan adequater worden besloten of een transfusie nodig is (bv. als het Hb vooraf de biopsie al laag was, kan dit mogelijk worden geaccepteerd). Bij afname van het Hb na biopsie dient ook een kruisbloed en bloedgroep te worden bepaald voor een eventuele bloedtransfusie.
3.1.4 Herhaal bij opname de stollingstesten (PTT, aPTT en bij VKA gebruik ook de INR) alleen bij gebruik van VKA of indien de laatste controle > 2 weken geleden is (practice point).
Onderbouwing:
De stollingstesten moeten bij opname worden herhaald als deze > 2 weken tevoren voor het laatst zijn bepaald of indien de patiënt VKA gebruikt ter controle of de INR voldoende is gecorrigeerd. Indien er sprake is van een verlengde stollingstest(en) kan geprobeerd worden de stolling te verbeteren (zo nodig in overleg met hematoloog). Patiënten met een verlengde INR kunnen in spoed situaties worden gecoupeerd maar indien de biopsie geen spoed behoeft wordt de voorkeur gegeven aan uitstel van de biopsie.
3.2.1 Overweeg patiënten na de nierbiopsie 24 uur in het ziekenhuis te observeren indien er sprake is van: reisafstand > 30 minuten, overmatig angstig zijn voor de biopsie en/of kwetsbaarheid (frailty) (practice point).
Onderbouwing:
De mate van kwetsbaarheid kan worden beoordeeld met één van de gevalideerde frailty scores waarmee ervaring is in het centrum.
3.2.2 Overweeg om patiënten met een hoog risico voor complicaties 24 uur lang na de biopsie te observeren in het ziekenhuis. Dit zijn patiënten met een eGFR < 30 ml/min, hypertensie voorafgaand aan de biopsie, Hb < 6 mmol/l en/of tromboycten < 100 × 109/l voorafgaand aan biopsie, patiënten met afwijkende stollingstesten, noodzaak tot overbrugging van de antistolling middels LMWH of indien er een indicatie is tot snel herstarten van anticoagulantia (2C).
Onderbouwing:
In de literatuur zijn bovenstaande risicofactoren geïdentificeerd als risico verhogend op een bloedingscomplicatie. Uiteraard heeft het bij patiënten die niet volledig voldoen aan één van deze criteria, maar wel veel co-morbiditeit hebben of bijvoorbeeld onder acetylsalicylzuur worden gebiopteerd, de voorkeur om ze 24 uur te observeren. Vaak zijn dit patiënten die zich al in een klinische setting bevinden waarbij verlenging van de observatieduur al logischerwijze plaats zal vinden. Alhoewel de trombocyten > 50 × 109/l dienen te zijn voor de biopsie, zijn de meeste studies verricht bij patiënten met trombocyten > 100 × 109/l. Derhalve suggereert de RLC dat patiënten met trombocyten < 100 × 109/l 24 uur ter observatie opgenomen moeten worden. Het preventief geven van desmopressine bij thrombocyten < 100 × 109/l is niet bewezen en wordt derhalve niet geadviseerd. Patiënten met Hb < 6 hebben weinig reserve bij een eventuele bloeding en kan er worden overwogen om deze patiënten ook langer te observeren.
3.2.3 Observeer laag-risico patiënten na een ongecompliceerde biopsie gedurende 8 uur in het ziekenhuis. Indien zij niet voldoen aan de punten genoemd in 3.2.1 kunnen zij met goede instructies met ontslag (1B).
Onderbouwing:
Hogan et al.8 adviseert op basis van de literatuur dat een observatieduur van minimaal 8 uur voldoende is om > 90% van de complicaties te detecteren. Bovendien worden complicaties na biopsie ook in een later stadium (> 72 uur) gerapporteerd. Derhalve kan een laag-risico patiënt na 8 uur observatie na een ongecompliceerde biopsie met ontslag (bloeddruk regulatie binnen streefwaarde, goed te instrueren patiënt).
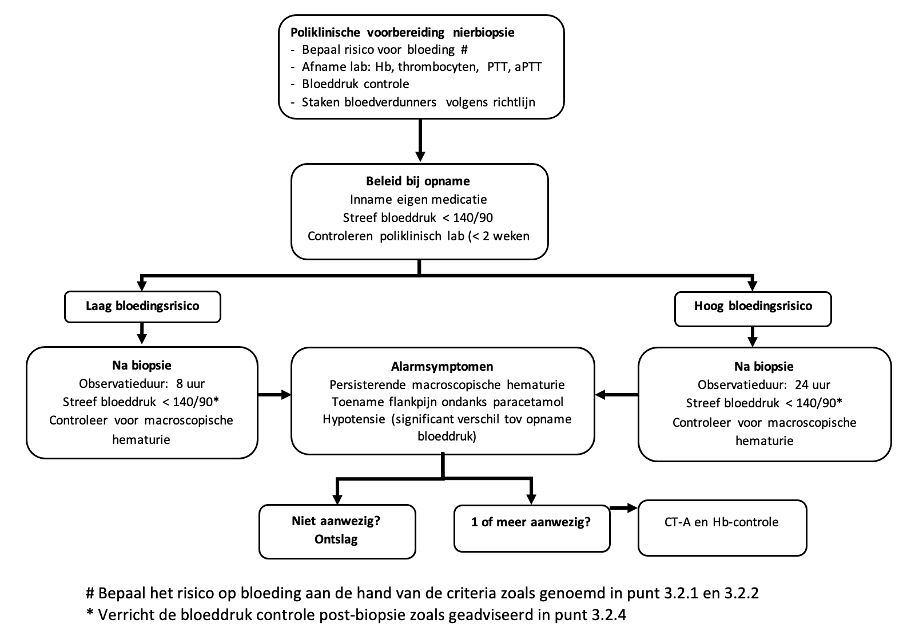
3.2.4 Controleer de eerste 2 uur na de biopsie intensief de vitale parameters (bijvoorbeeld a 30 minuten) in combinatie met strikte bedrust. Nadien kan het interval worden verlengd naar controles elk uur. Na 3 uur bedrust kan de patiënt in bed voorzichtig mobiliseren en na 6 uur kan de bedrust opgeheven worden. Verder dient de verpleegkundige de patiënt te controleren op ernstige flankpijn, spontane mictie en de aanwezigheid van macroscopische hematurie (practice point).
Onderbouwing:
Indien er een significante bloeddrukdaling optreedt of de patiënt ernstige flankpijn heeft dient er met spoed een CT-A te worden verricht om een bloeding te detecteren en indien aanwezig direct een coiling te verrichten (Hoofdstuk 4).
3.2.5 Verricht niet standaard een echo van de nier na een biopsie als screening voor (asymptomatische) hematomen (2C).
Onderbouwing:
De RLC acht het niet zinvol om een echo van de nier te (laten) verrichten na een biopsie als screening voor (asymptomatische) hematomen. Hogan et al.7 en Fraser et al.5 rapporteren dat een peri-renaal hematoom bij 57-91% van de patiënten zichtbaar is met een CT-scan en bij 70% met een echo. Het percentage klinisch relevante bloedingen echter slechts ongeveer 5%.
3.2.6 Verricht niet routinematig een serum Hb controle of urineonderzoek naar de aanwezigheid van microscopische hematurie na een ongecompliceerde biopsie (2C).
Onderbouwing:
De RLC acht het NIET zinvol om na een ongecompliceerde biopsie routinematig een serum Hb controle of urine onderzoek naar microscopische hematurie te verrichten. Een bloeding na nierbiopsie naar het pyelum zich uitend in macroscopische hematurie is meestal self-limiting waarbij het denkbaar is dat microscopische hematurie > 24 uur detecteerbaar blijft. Het standaard verrichten van een urine onderzoek binnen een dag lijkt dan ook niet bijdragend. Verder is er geen bewijs dat het routinematig verrichten van een Hb controle de uitkomst van een patiënt bij een eventuele complicatie verbetert. Het leidt wel tot een langere observatieduur en eventuele (onnodige) bloedtransfusie. Wel is beschreven dat patiënten met een anemie voorafgaand aan biopsie een hogere kans hebben op een significante anemie wat een transfusie vereist.
3.2.7 Geef patiënten bij ontslag mondelinge en schriftelijke informatie waarin duidelijk wordt beschreven welke klachten er kunnen optreden en welk telefoonnummer er gebeld kan worden in geval van nood (practice point).
Onderbouwing:
Patiënten dienen een document mee te krijgen met goed te begrijpen informatie welke bij ontslag nog mondeling moet worden toegelicht. De alarmsymptomen die moeten worden vermeld zijn: toename pijn in de flank, macroscopische hematurie, loze aandrang, koorts, onwel voelen. Zie bijlage 1 voor een voorbeeldtekst.
3.2.8 Instrueer patiënten om na een ongecompliceerde biopsie minimaal 1 week geen zware lichamelijke inspanning te leveren (practice point).
Onderbouwing:
Hoewel hierover geen data beschikbaar is acht de RLC het zinvol om dit advies te geven aan de patiënt.
4.1 Overweeg om bij verdenking op een milde tot ernstige bloeding (hypotensie en/of ernstige flankpijn) direct intraveneuze vochtsuppletie te starten waarna met spoed beeldvorming verricht dient te worden (practice point).
Onderbouwing:
De RLC adviseert om niet routinematig (echografisch) te screenen voor een hematoom omdat deze nagenoeg altijd aanwezig zal zijn. Indien er verdenking is op een bloeding zoals eerder beschreven verdient het de voorkeur om direct een CT-A te verrichten.
4.2 Verricht bij verdenking op een bloeding een spoed CT-A in plaats van een echo zodat de radioloog direct de mogelijkheden voor een eventuele interventie kan beoordelen (practice point).
4.3 Verricht radiologische danwel chirurgische interventie (afhankelijk van de lokale expertise) indien er sprake is van een actieve bloeding op de CT-A (1C).
4.4 Zorg dat er met spoed chirurgische interventie wordt verricht (waarbij zoveel mogelijk “niersparend” geopereerd moet worden) indien de bloeding niet succesvol gecontroleerd wordt met behulp van een radiologische interventie (practice point).
Onderbouwing:
Indien dergelijke chirurgische interventies niet mogelijk zijn in het centrum dan verdient het de voorkeur om de patiënt na stabilisatie zo snel mogelijk over te plaatsen naar een centrum met de juiste expertise.
Onderstaande tekst betreft een voorbeeld dat moet worden aangepast aan de lokale situatie en overlegd moet worden met de afdeling radiologie, als de nierbiopsie door de radioloog uitgevoerd wordt.
In overleg met uw behandelend arts heeft u besloten een nierbiopsie te laten verrichten. In deze folder krijgt u meer informatie over wat een nierbiopsie inhoudt.
Wat is een nierbiopsie?
Een nierbiopsie is een onderzoek waarbij de arts met een speciale naald enkele stukjes weefsel ter grootte van een halve lucifer uit de nier neemt.
Wat is het doel van een nierbiopsie?
Een nierbiopsie wordt uitgevoerd om de oorzaak van een nierprobleem, zoals achteruitgang van de nierfunctie of verlies van bloed en/of eiwit in de urine te achterhalen. Als de oorzaak bekend is, kan de arts de juiste behandeling geven.
Complicaties
De nier is een rijk doorbloed orgaan. Hierdoor bestaat de kans dat er door de biopsie een bloeding optreedt. Om deze kans te verkleinen, worden voor het onderzoek voorbereidingen getroffen. Na de nierbiopsie moet u opgenomen blijven om u goed in de gaten te kunnen houden. Meestal betreft het een kleine bloeding, die gepaard kan gaan met plaatselijke pijn en ongemak. In zeldzame gevallen (<1%) kan er een belangrijke bloeding optreden waarvoor bloedtransfusie nodig is. In het ergste geval is een ingreep nodig om de bloeding te stoppen. Daarnaast kunt u bloed in de urine hebben na een biopsie. Dit is meestal kortdurend en niet ernstig.
Voorbereiding
U wordt voor de behandeling opgenomen in het ziekenhuis. De duur van deze opname zal door uw behandelend arts worden bepaald en kan variëren van 8 uur (dagopname) tot 24 uur. U mag op de ochtend van de biopsie een licht ontbijt nuttigen. Als u op de afdeling bent, wordt u geadviseerd om tot 2 uur na de nierbiopsie nuchter te blijven. U mag, indien de arts dit heeft aangegeven, de medicijnen innemen die u gewend bent. Als u bloedverdunners gebruikt, dan moet u in overleg met uw arts hier een aantal dagen voor het onderzoek mee stoppen. Onder bloedverdunners vallen bijvoorbeeld de volgende medicijnen:
Acenocoumarol (sintrommitis), Fenprocoumon (marcoumar), Acetylsalicylzuur (Ascal), Clopidogrel (Plavix), Prasugrel (Efient), Ticagrelor (Brilique), Dabigatran (Pradaxa), Rivaroxaban (Xarelto), Apixaban (Eliquis), Ibuprofen (Advil, Brufen) en Diclofenac (Voltaren). Als u toch bloedverdunners heeft ingenomen, dan moet u dit voor de biopsie melden aan de arts en de verpleging.
Op de afdeling
U moet zich melden op de afgesproken tijd op de afdeling. Het is fijn om wat makkelijk zittende kleding mee te nemen naar het ziekenhuis. Deze kleding kan u dan voor het onderzoek aantrekken.
Voordat het onderzoek plaatsvindt, wordt er op de verpleegafdeling eerst bloed geprikt om te kijken of uw bloed voldoende snel stolt. Daarnaast wordt uw bloeddruk gemeten. Hierdoor wordt de kans op een bloeding beperkt. Aan de hand van deze uitslagen wordt beoordeeld of het onderzoek definitief door kan gaan.
Het onderzoek
De biopsie wordt uitgevoerd door de radioloog of de nefroloog. U wordt gevraagd of u in buik- (en soms zij)ligging wilt gaan liggen. Met een echoapparaat (dit is een apparaat dat werkt met geluidsgolven, hier voelt u niets van) wordt de ligging van de nier en juiste biopsieplaats bepaald. Tijdens het onderzoek is het belangrijk dat u zo stil mogelijk blijft liggen op het bed en de instructies met betrekking tot de ademhaling (rustig doorzuchten en op aangeven van de arts de adem vasthouden) op te volgen. Het gebied rondom deze plaats wordt goed schoongemaakt met een desinfecterende vloeistof. Vervolgens wordt de huid en onderhuidse weefsel verdoofd door met een naald verdovingsvloeistof rondom de biopsieplaats te spuiten. Daarna maakt de arts een klein sneetje in de huid voor de biopsienaald. Met behulp van de biopsienaald wordt een klein stukje weefsel uit de nier gehaald voor laboratoriumonderzoek. Het aanprikken van de nier kan wel een wat vervelend gevoel geven. Hevige pijn tijdens het aanprikken komt echter vrijwel niet voor. Via het insteekgaatje worden meestal twee tot drie biopsies verricht, zodat er voldoende weefselmateriaal is voor een beoordeling. Het onderzoek duurt ongeveer 30 minuten.
Na het onderzoek
Om de kans op een nabloeding te verminderen, heeft u na het onderzoek 3 uur platte bedrust. U ligt hierbij op uw rug. Als de verdoving is uitgewerkt, kunt u wat pijn krijgen op de biopsieplaats. Dit is een normaal verschijnsel. Als de (pijn)klachten toenemen of niet verminderen, dan moet u dit melden aan de verpleging. Op de afdeling meet de verpleegkundige op vaste tijden na de nierbiopsie de bloeddruk, pols en temperatuur. Daarnaast wordt er gekeken of de punctieplaats heeft doorgelekt en of er bloed in de urine aanwezig is. Na 3 uur platte bedrust mag u in bed geleidelijk wat mobiliseren. Indien er geen aanwijzing voor een nabloeding is, dan wordt na 6 uur uw bedrust opgeheven en mag u voorzichtig over de afdeling bewegen.
Ontslag
Mocht u alleen opgenomen zijn voor de nierbiopsie, dan mag u afhankelijk van het risico op bloeding dezelfde dag of pas de volgende dag met ontslag als de urine helder is en u zich verder goed voelt. Het is belangrijk om te weten dat u gedurende 7 dagen niet zwaar mag tillen. Krijgt u thuis toenemende pijnklachten, neem dan contact op met de afdeling Nefrologie.
Uitslag
Bij ontslag vanaf de afdeling krijgt u een afspraak voor de polikliniek mee als u die nog niet had, voor 1 – 2 weken na de nierbiopsie.
Tot slot
De informatie in deze folder is algemeen van aard. Dat wil zeggen dat het onderzoek is beschreven zoals dit meestal verloopt. Het kan zijn dat de arts een andere werkwijze kiest, die beter aansluit bij uw situatie. Het is niet mogelijk in deze folder alle varianten en alternatieven te vermelden. Ook risico’s en bijwerkingen zijn in algemene zin aangegeven.
Contact
Bij toename pijnklachten, koorts, loze aandrang, bloed in de urine en/of onwel voelen dient u contact op te nemen met de polikliniek nefrologie via ….tel nr….. of buiten kantoortijden met de spoedeisende hulp via ……tel nr……

© 2022. Alle rechten voorbehouden
Dr. T. Both, Maasstad ziekenhuis en ErasmusMC in Rotterdam
Dr. I.J.A.M Verberk-Jonkers, Maasstad ziekenhuis in Rotterdam
Dr. A.J. Varewijck, Maasstad ziekenhuis in Rotterdam
Dr. H.W. van Hamersvelt, RadboudUMC in Nijmegen
Dr. A.Y. Adema, Medisch Centrum Leeuwarden in Leeuwarden
Namens Nederlandse Federatie voor Nefrologie richtlijnencommissie verantwoordelijk:
Dr. A.J. Varewijck